责编丨迦溆
IVF/ICSI技术最关键的环节是受精卵的形成,代表着生物学新生命的开始。成熟的卵母细胞与获能的精子融合后分别形成雌原核和雄原核,标志着受精卵的形成。随后,两个单倍体原核迁移并彼此聚集,经过第一次卵裂后形成二细胞胚胎,完成从减数分裂到有丝分裂的过渡,而后经过几次连续的的有丝分裂和分化后形成囊胚,植入子宫以建立正常妊娠。然而,据统计通过辅助生殖技术所获得的胚胎中大约10%阻滞在卵裂早期阶段;其中大约有2%的胚胎阻滞在受精卵阶段,不能完成第一次卵裂过程,即“卵裂障碍”。临床上表现为卵裂障碍的不孕患者通常经过反复多次的体外助孕治疗均无法获得可移植的胚胎,亦无有效的治疗方法,给患者和家庭带来了巨大的精神压力和经济负担,导致离婚率攀升。据估计,约有一半的不孕病因涉及遗传因素,然而导致人类不孕的大多数遗传原因仍不明晰。
2021年5月6日,山东大学陈子江院士团队赵涵课题组在Cell Research杂志发表题为Dominant mutations in CHK1 cause pronuclear fusion failure and zygote arrest that can be rescued by CHK1 inhibitor的研究论文。研究发现CHK1是导致以雌雄原核融合障碍为主的人类卵裂障碍致病基因,并阐明了致病机制,通过一系列体内与体外研究发现CHK1抑制剂可以有效挽救小鼠和人类的受精卵阻滞表型,为此类不孕症患者的治疗提供有效和安全的干预措施。

研究人员在四个卵裂障碍家系中发现了细胞周期检查点激酶1 CHK1( checkpoint kinase 1,简称“CHK1”或“CHEK1”)杂合变异,患者的受精卵绝大多数阻滞在一细胞阶段,并且伴有明显的原核融合障碍(PFF-ZA)。该基因突变呈现表型仅累及女性的常染色体显性遗传模式,与团队前期发现的ZP3常染色体显性突变可导致卵母细胞退变的遗传模式一致。根据ACMG遗传变异分类标准与指南,以上4个CHK1突变评分均为可能致病。
进化上高度保守的DNA损伤反应和细胞周期检查点保证了基因组稳定性,其中起中心作用的是CHK1,可参与几乎所有的细胞周期检查点。最早在裂殖酵母中发现CHK1可调控G2/M期转换,后续发现其在基因组稳定性、癌症治疗、早期胚胎发育等方面均发挥重要作用。研究显示,CHK1在受精卵阶段以及受精前后阶段相对高表达,表明其在受精卵阶段可能发挥重要作用。研究人员将这4个人类CHK1突变体显微注射至小鼠受精卵后发现,小鼠受精卵也发生雌雄原核融合受阻、不能卵裂,完全重复了人类PFF-ZA的表型。
CHK1蛋白的N端是高度保守的激酶结构域,C端为调节结构域,包含两个保守基序(CM1与CM2)。既往研究表明,CM1与CM2内的某些突变可以改变CHK1蛋白构象,导致其激酶活性增高。有趣的是,这4个CHK1有害突变分别位于C端的CM1和CM2内或附近。体外实验显示突变后蛋白在胞内的定位改变,蛋白结构预测表明突变改变与周围氨基酸残基间的氢键与蛋白的表面电势,进一步的体外激酶活性检测表明突变后CHK1激酶活性增强。已有研究提示,激活后的CHK1可通过磷酸化下游CDC25C导致抑制性CDK1积聚,进而引起细胞周期G2/M期转换阻滞。与之一致的是,突变CHK1可导致抑制性磷酸化的CDC25C(S216)与CDK1(T14&Y15)表达增多,尤其以截短突变(p.F441fs*16)最为显著;并且将CDC25C与CDK1的关键磷酸化位点突变后,可显著提高携带突变受精卵的卵裂率,表明CHK1激活突变通过CDC25C/CDK1通路导致受精卵G2/M期转换阻滞,引发卵裂障碍。
目前,绝大多数卵裂障碍患者的病因仍不明晰,亦缺乏有效的治疗手段,探索切实可行的治疗方案将为该类患者与其家庭带来福音。CHK1抑制剂广泛报道到与多种抗癌药物联合应用用于增强肿瘤细胞对放化疗的敏感性。鉴于CHK1突变蛋白的激酶活性增高,研究人员选择了一种ATP竞争性的CHK1抑制剂(PF477736)进行体外挽救实验,该抑制剂目前已有一期临床试验,与吉西他滨联合应用治疗肿瘤。体外实验表明合适浓度的CHK1抑制剂可通过降低CHK1下游磷酸化CDC25C与CDK1的水平显著提高突变小鼠受精卵的卵裂率与囊胚形成率并可获得健康小鼠后代。有幸的是,患者捐赠科研的受精卵应用CHK1抑制剂处理后可发育形成囊胚(下图)。进一步研究发现,这些囊胚来源的胚胎干细胞具有全能性并且保持了基因组的完整性。
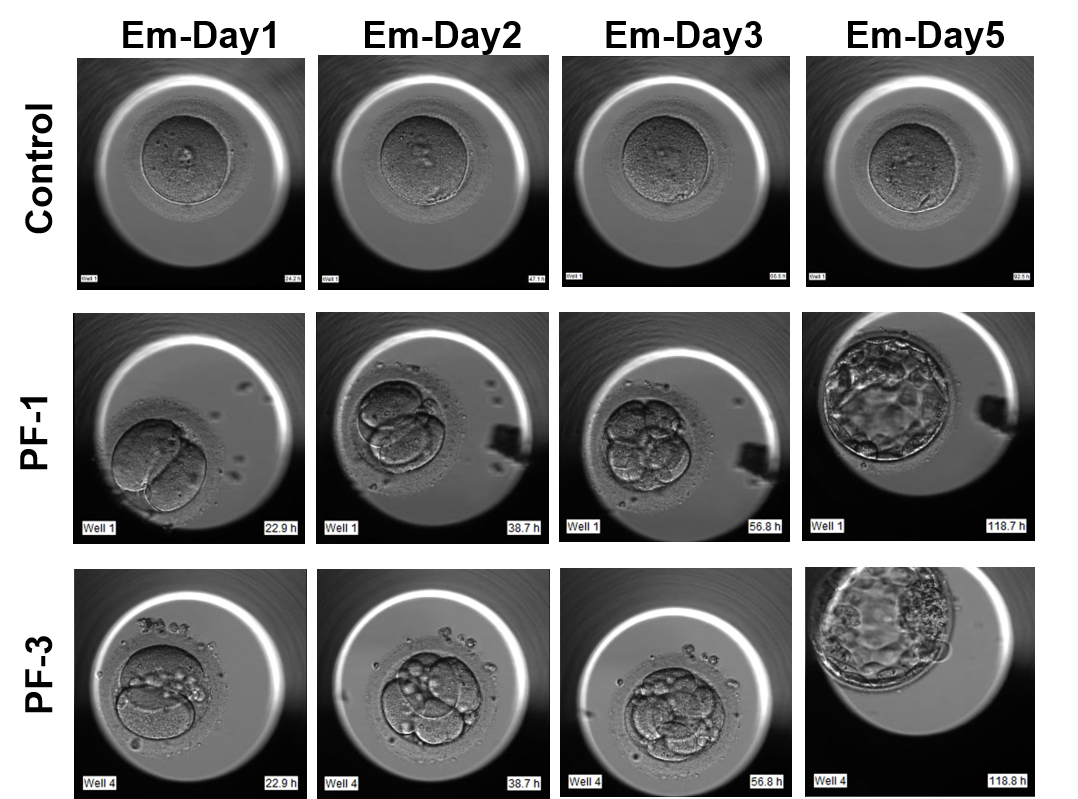
应用CHK1抑制剂PF477736可使患者受精卵发育至囊胚
本研究发现CHK1 C末端保守结构域内的显性突变可导致原核融合失败与受精卵发育阻滞(PFF-ZA),并阐明了突变引起的CHK1激酶活性增加阻碍了受精卵的G2/M转换。重要的是,使用CHK1抑制剂抑制其激酶活性可以有效挽救小鼠和人类的受精卵阻滞表型,为此类不孕症患者的治疗提供有效和安全的干预措施。
与此同时,清华大学医学院那洁课题组与安徽医科大学曹云霞和章志国教授课题组及首都医科大学附属北京妇产医院助理研究员李琳,于Protein & Cell在线发表题为“Maternal heterozygous mutation in CHEK1 leads to mitotic arrest in human zygotes”的论文。研究人员也发现了一个表现为受精卵分裂失败的雌性不育家系,该家系中不孕症患者存在CHEK1 R442Q的杂合突变。研究人员发现突变的Chk1蛋白同样造成了半数以上小鼠受精卵第一次有丝分裂的阻滞,且体外纯化的突变体CHEK1激酶活性比野生型CHEK1稍高。

那洁/曹云霞/章志国/李琳团队将研究重点聚焦于DNA损伤反应。升高的CHEK1激酶活性使得第一个有丝分裂检查点阈值过高,在不存在DNA损伤或错误的情况下细胞周期依然无法向下进行。研究者发现低剂量的CHEK1抑制剂可以让表达Chk1 R442Q的小鼠受精卵分裂,并未造成更多的DNA损伤,且发育到囊胚的胚胎有同样多的表达Oct4和Nanog的内细胞团细胞。对处理后的胚胎转录组测序表明,CHEK1抑制剂的处理也未造成显著的转录组改变。该研究揭示了人类早期胚胎第一次有丝分裂对DNA损伤检查点调控极其敏感,并提示人类和小鼠的卵子到受精卵转化过程有种属特异性。以上两个团队独立的研究互为佐证,相辅相成。
陈子江院士与赵涵教授为Cell Research论文的通讯作者。山东大学张鸿惠博士、上海交通大学陈泰来博士、山东大学吴克良教授、侯真真助理研究员为共同第一作者。
那洁副教授、曹云霞教授、章志国教授,李琳博士为Protein & Cell 论文的通讯作者。安徽医科大学附属医院陈蓓丽博士、清华大学医学院博士后郭健颖、博士生王婷为论文共同第一作者。清华大学医学院李海涛教授指导了CHEK1蛋白纯化和激酶活性检测实验。
原文链接:
https://www.nature.com/articles/s41422-021-00507-8
https://link.springer.com/article/10.1007/s13238-021-00844-9

