2025年2月14日,安徽医科大学第一附属医院生殖中心/国家卫健委配子及生殖道异常研究重点实验室曹云霞教授和上海交通大学医学院附属第一人民医院贺小进教授研究团队在生殖医学顶级期刊Human Reproduction Update(5年影响因子:17.8)发表了题为“Defects in mRNA splicing and implications for infertility: a comprehensive review and in silico analysis”的系统性综述。mRNA的选择性剪接是蛋白质翻译前的关键环节,由顺式作用元件与反式作用因子协同完成。文章荟萃了生殖障碍相关的顺式作用元件核苷酸序列变异与反式作用因子功能缺陷。同时,也介绍了作者多年来在mRNA剪接这一领域积累的国际先进研究成果。通过对mRNA剪接缺陷与生殖障碍的发生及导致不孕不育的机制进行了全面深入的论述,为疑难的男性、女性生殖障碍疾病的诊断与治疗提供了新视角和中国经验。
mRNA剪接是调控转录后基因表达、核输出和翻译的关键过程,涉及内含子的精确去除和外显子的连接。生殖系统通过mRNA剪接,调控生殖发育、内分泌、减数分裂、有丝分裂和配子功能,以维持生殖细胞生成、受精、胚胎发育、着床和妊娠。例如,睾丸表达超过80%的蛋白编码基因,且存在高水平的选择性剪接事件,对配子发生中的有丝分裂和减数分裂至关重要。在小鼠精子发生中,高通量测序揭示了剪接调节因子(如Ranbp9和Morf4l1)的基因表达动态,以及生殖系统中的mRNA选择性剪接事件(如Spo11和Dmc1)。
在分子水平上,顺式作用元件与反式作用剪接因子的复杂相互作用对mRNA选择性剪接至关重要。顺式作用元件是前体mRNA中外显子或内含子中的短核苷酸序列。顺式作用元件包括启动子、增强子和沉默子等,是反式作用因子的结合位点。反式作用因子包括剪接体蛋白、剪接因子及其他相关的RNA结合蛋白,其核心是包含300多个组分的剪接体。剪接体分为U2和U12两种,分别识别GT-AG和AT-AC/GT-AG剪接位点。除剪接体相关蛋白外,其他剪接因子(如富含丝氨酸/精氨酸的蛋白和异构核糖核蛋白)也会结合外显子和内含子区的增强子和沉默子元件,参与剪接体组装和剪接位点选择。
在过去五年中,研究发现大量反式作用剪接因子功能异常导致模型生物不育。然而,人类不育中与异常剪接过程相关的反式作用剪接因子和顺式作用元件的致病变异尚未系统综述。另外,随着高通量测序和分子功能注释技术的发展,针对顺式作用元件剪接变异的预测工具不断涌现。这些工具可用于重新评估可能影响mRNA选择性剪接和基因功能的人类不育相关致病变异,这些变异在最初研究中可能被错误分类。
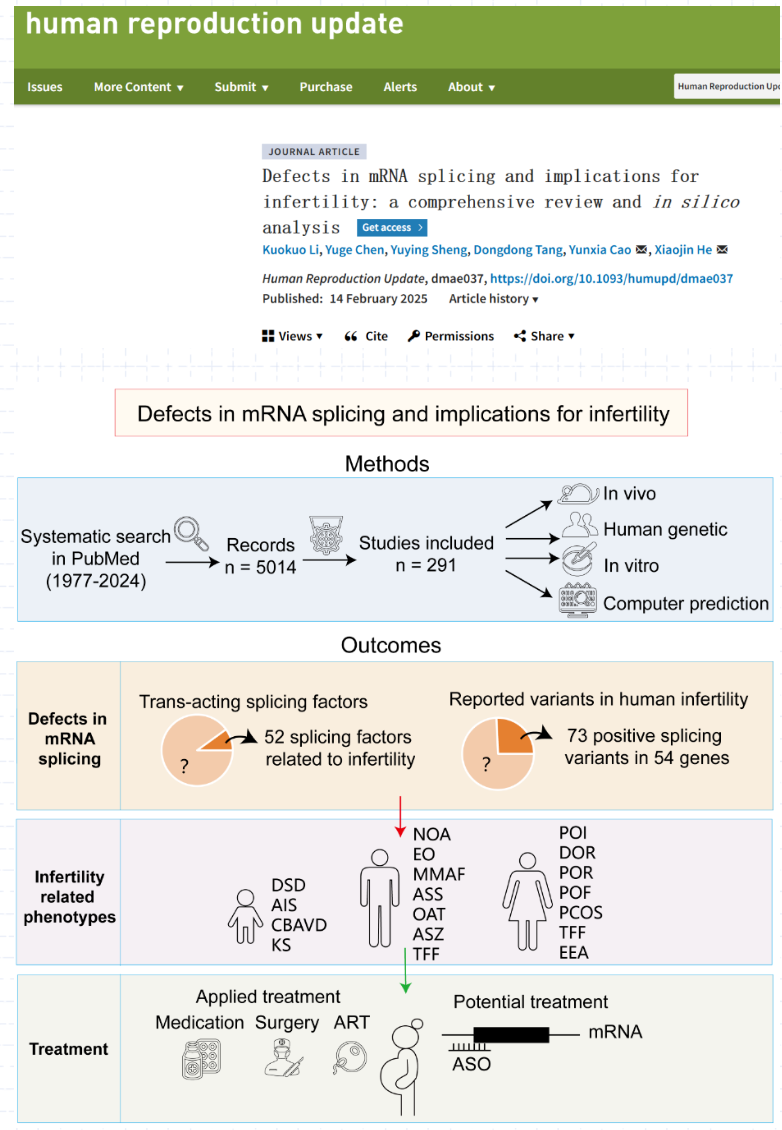
研究团队从mRNA缺陷与生殖发育关系的角度出发,分别从剪接体组成组装、RNA结合蛋白、剪接相关表观遗传调控、人类剪接调控蛋白变异、已报道人类基因组剪接变异等多个层次分析与生殖障碍之间的关系。比如,目前分别有52个剪接调控蛋白功能异常和72个剪接变异被报道和生殖障碍有关。然而,仍然有剪接调控蛋白与生殖障碍疾病之间的关系不清楚,需要进一步通过动物模型来验证。另外,目前已经报道的大量生殖障碍疾病相关变异的具体发病机制不清楚,其中一部分变异可能通过影响mRNA选择性剪接导致疾病的发生。研究团队进一步系统汇总了剪接变异预测工具,其中SPCards(http://www.genemed.tech/spcards/home)为研究团队前期开发的剪接变异整合分析平台。SPCards纳入18款剪接变异分析工具,在全基因组水平识别导致剪接异常的基因变异(包括非经典剪接位点)。另外,团队系统介绍了剪接异常相关的功能实验验证方法,为后续研究剪接变异与生殖障碍疾病之间的关系提供研究策略。
为进一步推动剪接缺陷与生殖障碍疾病之间关系的探索,研究团队提出如下建议:首先越来越多的与生殖障碍相关的反式作用剪接蛋白在最近几年被报道,未来有望进一步明确剪接调控蛋白在生殖中的作用及其机制。其次,剪接相关蛋白的敲除或敲低导致模型生物的不育,但目前仅在少数蛋白中发现人类致病变异。需进一步研究以确定这些蛋白是否为人类不育的致病因素。另外,顺式作用元件变异对人类不育的临床影响可能被严重低估,可能是由于常规遗传分析中遗漏了大量的剪接变异。亟需开发剪接变异精确筛选方法,以发现可能被忽视的非经典剪接变异。最后,研究聚焦于开发针对异常mRNA剪接的生殖障碍剪接调控疗法,为目前缺乏有效治疗方案的疑难患者提供新的治疗选择。

