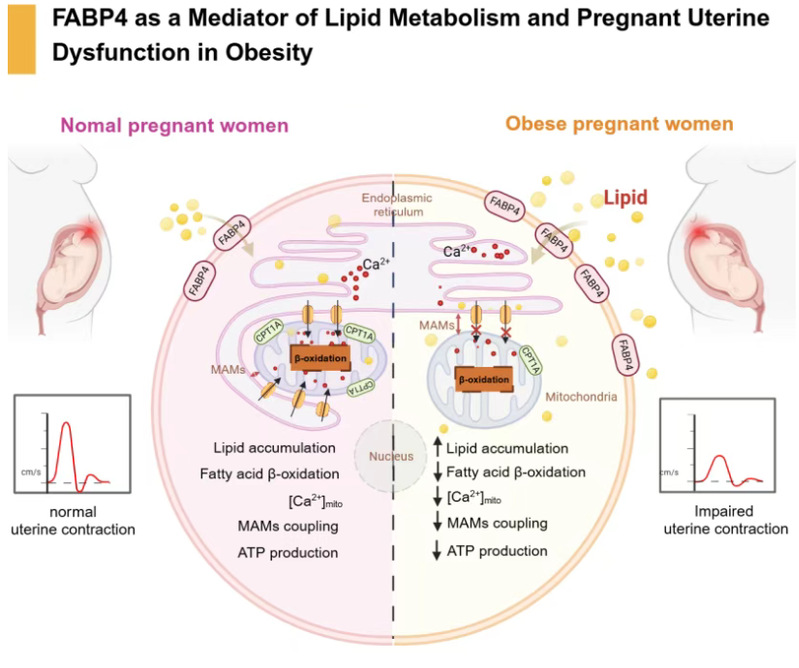
2025年4月7日,安徽医科大学第一附属医院妇产科/国家卫健委配子及生殖道异常研究重点实验室曹云霞/尹宗智教授团队在国际知名学术期刊《先进科学》(Advanced Science, IF=14.3)上在线发表题为FABP4 as a Mediator of Lipid Metabolism and Pregnant Uterine Dysfunction in Obesity (DOI: 10.1002/advs.202501077)的研究成果。该研究首次揭示,肥胖孕妇在妊娠晚期易患子宫平滑肌功能障碍,然而其具体发病机制尚未明确。研究发现,肥胖孕妇、高脂饮食(HFD)诱导的肥胖小鼠,以及棕榈酸(PA)处理的子宫平滑肌细胞(USMCs)中,脂肪酸结合蛋白4(FABP4)的表达水平显著升高。FABP4作为细胞内脂肪酸转运的关键介质,在脂肪酸从细胞外运输到细胞内过程中发挥重要作用。
进一步研究发现,肥胖促进了脂肪酸的过量摄取,导致USMCs中脂质异常堆积并伴随腺苷三磷酸(ATP)生产效率降低。这一病理过程源于线粒体相关膜(MAMs)的耦联减弱,而MAMs在钙离子、脂质及营养物质交换中至关重要。此外,通过腺病毒注射提高FABP4表达水平,可在正常饮食小鼠中模拟HFD小鼠的相关效应。本研究发现不仅揭示了FABP4在肥胖相关子宫平滑肌功能障碍中的关键作用,更为改善肥胖孕妇分娩结局提供了潜在的治疗靶点。

立足临床 提出问题
全球肥胖率持续上升已成为一项严峻的公共卫生危机,并对人类社会的可持续发展构成重大威胁。与此同时,育龄女性中的肥胖率也随整体肥胖人群扩大而上升,这一现象备受生殖健康领域的关注。现有观察性研究已经证实,孕妇肥胖与不良妊娠结局之间存在显著关联,这些不良结局涵盖子痫、妊娠期糖尿病及胎膜早破等严重并发症。值得注意的是,许多与肥胖相关的并发症与围产期子宫收缩功能受损有关,肥胖孕妇在分娩过程中面临更高的子宫收缩力下降的风险。然而,肥胖导致子宫平滑肌功能障碍的具体分子机制仍未得到充分阐明。
科学设计 逐层分析
研究人员分别采集了肥胖和非肥胖孕妇的子宫肌条,以及高脂饮食(HFD)或正常饮食(ND)喂养的妊娠小鼠的子宫肌条进行对比。结果显示,肥胖组的子宫收缩频率较低,收缩峰值显著减少。通过计算曲线下面积(AUC)与肌肉条重的比值(AUC/g),发现肥胖组的子宫收缩强度低于对照组。此外,研究还对妊娠晚期小鼠的子宫平滑肌细胞(USMCs)进行了分离和纯化,并建立了永生化的细胞系。Nile Red染色结果表明,这些细胞内存在明显的脂质积累,同时伴随脂肪酸氧化(FAO)水平的下降。胶原收缩实验进一步证实,经过棕榈酸(PA)处理的细胞在高KCl和催产素刺激下的收缩能力显著减弱。
线粒体作为细胞的能量工厂,通过合成三磷酸腺苷(ATP)为各类细胞代谢活动提供能量支持。尤其是在子宫平滑肌收缩过程中,线粒体钙离子(Ca2+)信号通路在调节肌肉收缩与舒张中至关重要,需要与动作电位产生和ATP供应协调工作。研究发现,PA处理的USMCs表现出线粒体钙离子流入减少和线粒体膜电位受损,提示线粒体功能受损与肥胖导致的子宫收缩功能减弱相关。线粒体功能依赖于正常的脂质代谢,而这主要通过线粒体磷脂合成和来自内质网的脂质转运维持。研究发现,HFD或PA处理会增加USMCs中内质网与线粒体的距离,削弱IP3R1-GRP75-VDAC1复合体的相互作用,减少内质网到线粒体的钙离子流动,可能抑制妊娠期子宫收缩。值得注意的是,Mfn2作为维持内质网与线粒体连接的核心分子,其功能缺失会导致内质网应激,破坏线粒体代谢、胰岛素信号通路和能量稳态。上调MAMs连接蛋白Mfn2可以恢复FABP4介导的线粒体损伤,并增强子宫收缩。
得出结论 指导临床
本研究揭示了细胞器间通讯紊乱在肥胖所致线粒体功能障碍及子宫收缩减弱中的重要作用。通过4D-FastDIA蛋白组学分析,发现FABP4介导的胆固醇代谢通路在HFD喂养小鼠中显著上调。FABP4表达水平升高直接导致细胞内脂质积累、MAMs耦合减弱,进而影响子宫收缩,并且这种影响不依赖于肥胖状态。敲除FABP4基因可显著恢复子宫平滑肌的收缩能力,而Mfn2过表达则改善了线粒体功能。这些发现揭示了肥胖通过破坏子宫平滑肌能量代谢来影响分娩过程的机制,突出了FABP4和MAMs作为潜在治疗靶点的应用前景,为改善肥胖孕妇的分娩结局提供了新的干预思路和策略基础。
通讯作者介绍:
曹云霞



